中国药品监督管理局(CFDA,现为国家药品监督管理局NMPA)逐步优化药品审评审批流程,其中原料药与药品的共同审评审批是一个重要环节。这一改革旨在提高药品质量、降低企业成本,并加快药品上市速度。结合金融知识流程外包(KPO)的理念,可以更好地理解这一流程的高效性和协同性。
一、背景与意义
原料药是药品生产的核心组成部分,其质量直接关系到药品的安全性和有效性。传统的审评审批中,原料药和制剂药品需分别提交申请,导致时间成本高、资源浪费。共同审评审批制度通过整合申请资料,简化流程,提高了整体效率。金融知识流程外包作为现代服务模式,强调专业知识和流程优化,与药品审评的理念不谋而合,即通过标准化和外包思维提升管理效率。
二、CFDA共同审评审批流程详解(一图概览)
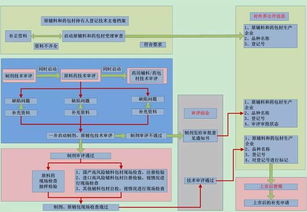
根据CFDA发布的流程图,共同审评审批主要包括以下步骤:
1. 申请提交:企业同时提交原料药和药品的申请资料,包括药学、非临床和临床数据。
2. 形式审查:CFDA对资料的完整性进行初步审核,确保符合要求。
3. 技术审评:专家团队对原料药和药品的质量、安全性和有效性进行同步评估,重点关注原料药的稳定性、杂质控制和与药品的相容性。
4. 现场检查:必要时,对原料药生产场地和药品生产企业进行现场核查。
5. 综合审评:基于技术审评和检查结果,形成综合意见,决定是否批准。
6. 审批决定:通过后,颁发药品注册证书和原料药关联审评通过证明。
整个流程强调数据共享和协同评估,减少了重复环节,通常可将审批时间缩短30%以上。
三、金融知识流程外包(KPO)的启示
金融KPO涉及将专业知识密集型流程外包给专业机构,以提升效率和准确性。在药品审评中,可以借鉴这一模式:
- 流程优化:通过外包思维,将部分审评环节(如数据分析和风险评估)委托给第三方专业机构,提高审评质量。
- 资源整合:类似于KPO中的知识管理,CFDA可以建立共享数据库,促进原料药和药品数据的互通,减少企业负担。
- 风险管理:应用金融领域的风险评估工具,加强对原料药供应链的监控,确保药品安全。
四、优势与挑战
共同审评审批的优势显而易见:加速药品上市、降低企业成本、提升监管效率。挑战也不容忽视,例如企业对流程的适应、数据标准化问题,以及监管资源的分配。借鉴金融KPO的经验,可以通过培训、技术支持和国际合作来应对这些挑战。
五、结语
原料药与药品共同审评审批是CFDA改革的重要举措,结合金融知识流程外包的理念,可以进一步推动药品产业的创新与发展。随着数字化和人工智能的应用,这一流程有望更加智能高效,为公众健康提供更强保障。企业应积极适应新规,加强内部管理,以抓住机遇。